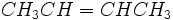میکروب شناسی آب
میکروب شناسی آب:
آبی که به صورت باران,تگرگ و برف بر سطح زمین می ریزد دارای میکروب های موجود در هواست .هنگام نزول باران مقدار قابل ملاحظه ای از میکروارگانیسم های هوا کاسته می شود.آب باران پس از شستن سطح خاک به طرف دریاچه ها و اقیانوس عا سرازیر می شود و میکروبهای هوا و خاک را با خود به طرف منابع طبیعی آب میبرد.آبی که از طبقات مختلف زمین عبور می کند و به قسمت های عمیق خاک میرود در مراحل مختلف اکثر میکروبهای خود را از دست می دهد. در حقیقت طبقات مختلف زمین مانند صافی عمل کرده جمعیت میکروبهای اینگونه آبها را کم می کنند.به طور کلی چون منشا آبهای مختلف با یکدیگر تفاوت دارند لذا نوع میکروارگانیسم های موجود در آنها نیز با هم متفاوت اند.
مباحث مختلف میکروب شناسی آب شامل میکروب شناسی اقیانوس ها ,دریاها,تالابها,حوضچه ها,نهرها,رودخانه ها,آب آشامیدنی و فاضلابهاست.
چون آب قادر به حمل میکروارگانیسم های مختلف است لذا می تواند یکی از عوامل مهم و اساسی مؤثر در بهداشت یک منطقه باشد.عوامل بیماریزا که توسط آب منتقل می شوند بیشتر در دستگاه گوارش بیماری تولید می کنند.عوامل بیماریزا در مدفوع افراد آلوده وجود دارند و چنانچه این عوامل در شرایطی از طریق فاضلاب ها با آب آشامیدنی تماس حاصل کنندباعث بروز بیماری در افراد سالم می گردد.آبی که فاقد میکروارگانیسم های بیماری زا و مواد شیمیایی زیان آور باشد “آب آشامیدنی” و آبی که به وسیله فاضلاب آلوده شده باشد “آب آلوده ” خوانده می شود.
تشخیص آلودگی آب از نظر باکتری شناسی:
آبی که کاملا شفاف و بدون بو و طعم است ممکن است آلوده به میکروارگانیسم باشد.آزمایشهای باکتری شناسی برای تشخیص میزان آلودگی آب فقط مربوط به تشخیص عوامل بیماری زای موجود در آب نیستزیرا عوامل بیماری زا به تعداد خیلی کم وارد آب می شوند و اکثراً پس از ورود به آب برای مدت طولانی قادر به ادامه زندگی نیستند .در نتیجه برای تشخیص آلودگی آب وجود گروهی از باکتری هاکه در حالت طبیعی در روده ی انسان و جانوران زندگی می کنند و به نام کلی فرم ها موسوم اند و همچنین استرپتوکوکوس فکالیس,کلاستریدیوم ولشی ای ,کلاستریدیوم پرفرژنس در آب جستجو می شوند.
تشخیص انواع ذکر شده در آب دلیل بر آلودگی آن توسط مدفوع است و از طرفی چون عوامل بیماری زا از طریق مدفوع افراد آلوده وارد آب می شوند,وجود و تشخیص انواعی از باکتری ها مانند کلی فرم ها در آب دلیل بر آلودگی آب توسط مدفوع است.انتخاب کلی فرم ها به ویژه گونه اشریشیاکلی به عنوان شاخص آلودگی به این علت است که این باکتری در روده ی آدمی به تعداد زیادی وجود دارد و در مقایسه با انواع باکتری های بیماری زا مدت طولانی تری در آب زنده می ماند.کلی فرم ها گروهی از باسیل های گرم منفی بدون هاگ هوازی یا بی هوازی اختیاری و تولید کننده ی گاز در محیط واجد لاکتوز هستند.نمونه های اصلی این گروه از باسیل ه عبارتند از اشریشیا کلی و انتروباکتر آئروژنز.
برای تشخیص آلودگی آب وهنگام نمونه برداری رعایت نکات زیر ضروری است:
۱- نمونه ها باید تحت شرایط سترون و در بطری های سترون گرفته شوند
۲- نمونه ها باید معرف مخزنی باشند آب از آن مصرف شده است
۳- هنگام نمونه برداری باید دقت شود آلودگی اضافی رخ ندهد
۴- جهت از بین بردن (خنثی کردن ) کل موجود در آب باید در داخل بطری نونه گیری قبل از استریلآن مقداری کریستال تیوسولفات سدیم ریخت
۵- نمونه ها باید هرچه زودتر پس از جمع آوری مورد آزمایش قرار گیرند و چنانچه آزمایش آب با تأخیر همراه باشدنمونه ها باید در دمای بین صفر تا ۱۰ درجه سانتی گراد نگه داری شوند.
آزمایش های باکتری شناختی که جهت تشخیص آلودگی آب انجام می شود عبارتند از:
۱- آزمایش برای تشخیص کلی فرم ها در آب
۲- شمارش تعداد باکتری های موجود در آن
شمارش تعداد باکتری ها در آب:
روش کار:
۱- برای شمارش تعداد باکتری ها در آب دو نمونه آب لوله کشی و آب نهر را انتخاب کرده
۲- در مورد آب نهر آن را تا رقت ⁵ ̄ ۱۰ رقیق کنید و آب لوله کشی را بدون رقیق کردن مورد استفاده قرار دهید
۳- از آب های مورد استفاده روی پلیت ها کشت می دهیم و پلت ها را ۴۸ ساعت در گرمخانه ی ۳۵ درجه سانتی گراد بگذارید سپس به بررسی و شمارش تعداد کلنی ها یا تعداد باکتری های موجود در ۱ سی سی از آب بپردازید.
از روی تعداد کلی باسیل های موجود در آب آبها را به سه دسته زیر تقسیم می کنند:
الف – آب بسیار خوب که در هر ۱۰۰ سانتی متر مکعب آن کمتر از یک اشریشیا کلی وجود دارد
ب – آب خوب که در هر ۱۰۰ سانتی متر مکعب آن یک تا دو اشریشیاکلی وجود دارد
ج – آب مشکوک که در هر ۱۰۰ سانتی متر مکعب آن بیش از ۱۰ اشریشیاکلی وجود دارد
تشخیص کلی فرم ها در آب:
برای شناسایی و شمارش کلی فرم ها محیط های انتخابی و افتراقی و روش خاصی لازم است.به این منظور دو روش اساسی شناخته شده است: الف – روش MPN (Most probable Number ) ب – روش فیلتر غشایی
الف – روش MPN :در این روش کلی فرم ها را در چند مرحله شناسائی می کنند: ۱- مرحله احتمالی ۲- مرحله تأییدی ۳- مرحله تکمیلی. در مرحله احتمالی رقت هایی از نمونه آب را به لوله های محتوی آبگوشت لاکتوز دار و معرف PH (لاکتوز فنل رد براث ) اضافه کرده و آنها را تا ۲۴ الی ۴۸ ساعت در گرمخانه قرار می دهند.تخمیر لاکتوز به اسید و گاز نشانه مثبت بودن واکنش است. در آزمایش احتمالی متداول در ۱۵ لوله حاوی محیط کشت نمونه آب را کشت میدهند (در هر یک از ۵ لوله اول ۱۰ میلی لیتر ,در ۵ لوله دوم یک میلی لیتر و در ۵ لوله سوم ۱/۰ میلی لیتر) .اگر اسید و گاز در هیچ یک از لوله ها پیدا نشود آب از نظر بهداشتی رضایت بخش در نظر گرفتته می شود و از نظر آماری این حالت نشانگر کمتر از ۲/۲ کلی فرم در هر ۱۰۰ میلی لیتر آب است .
هرگاه یک سری از لوله ها در آزمایش احتمالی نتیجه مثبت نشان دهند,تست اضافی انجام می گیرد زیرا میکروب های دیگری غیر از کلی فرم ها می توانند لاکتوز را با تولید گاز تخمیر نمایند. در آزمایش تأییدی از لوله های مثبت برداشت کرده و بر روی محیط افتراقی (ائوزین متیلن بلو آگار ) به طور خطی کشت می دهند.با توجه به اینکه کلی فرم ها از لاکتوز اسید تولید می کنند لذا کلنی هایی با مرکز تیره رنگ ایجاد می کنند .در عین حال اشریشیاکلی کلنی های بزرگ با مرکز تیره رنگ با درخشندگی ویژه,متمایل به سبز ایجاد می کند که علت ایجاد این درخشندگی یا جلای فلزی سبز ,آزاد شدن آزاد شدن ائوزین از محیط E.M.B و اکسید شدن آن در مجاورت هواست .ائوزین در محیط به صورت ترکیب با سولفیت سدیم است.در اثر رشد اشریشیاکلی از تخمیر لاکتوز ماده حدوسطی از جنس استالدئید تشکیل می شود که این ماده با سولفیت سدیم ترکیب شده سبب آزاد شدن معرف ائوزین می گردد.
پیدایش این نوع کلنی ها نشانگر مثبت بودن آزمایش تأییدی است.در آزمایش تکمیلی تک تک کلنی ها را از محیط تأییدی برداشت کرده و در آبگوشت لاکتوز دار و همچنین در محیط TSI ,24 ساعت در ۳۵ درجه قرار می دهند.هرگاه در این محیط ها اسید و گاز ایجاد شود و کلنی جدا شده گرم منفی , میله ای شکل و بدون اسپور باشد نتیجه آزمایش تکمیلی را مثبت اعلام می کنند.
ب)کلی فرم ها را همچنین می توان با روش فیلترهای غشائی نیز شناسایی کرد. بدین ترتیب ۱۰۰ میلی لیتر از آب مورد آزمایش را از فیلتر غشائی که قطر منافذ آن ۴۵/۰ میکرون است عبور می دهند.باکتری ها بر سطح فیلتر باقی می مانند,آنگاه پالایه را بر روی محیط کشت قرار می دهند.باکتری های کلی فرم بر روی فیلتر آغشته به ماده غذایی کلنی هایی مشخص رشد می کنند.هرگاه فقط یک کلنی از این ۱۰۰ میلی لیتر آب رشد کند آب را معمولاٌ از نظر آشامیدن سالم و بهداشتی می شناسند.
 زی درباکتری شناسی است که اولین بار توسط کریسین گرم ابداع شد . دراین رنگ آمیزی باکتریها بر مبنای رنگ باکتری پس ازرنگ آمیزی به دودسته گرم مثبت وگرم منفی تقسیم می شوند . رنگ باکتری پس ازرنگ آمیزی به توانایی حفظ رنگ اول وبه عبارتیبه ساختمان دیواره سلولی باکتری بستگی دارد . دررنگ آمیزی گرم باکتریهای گرم مثبت پس ازرنگ آمیزی به رنگ بنفش وباکتری های گرم منفی به رنگ قرمز مشاهده می شود
زی درباکتری شناسی است که اولین بار توسط کریسین گرم ابداع شد . دراین رنگ آمیزی باکتریها بر مبنای رنگ باکتری پس ازرنگ آمیزی به دودسته گرم مثبت وگرم منفی تقسیم می شوند . رنگ باکتری پس ازرنگ آمیزی به توانایی حفظ رنگ اول وبه عبارتیبه ساختمان دیواره سلولی باکتری بستگی دارد . دررنگ آمیزی گرم باکتریهای گرم مثبت پس ازرنگ آمیزی به رنگ بنفش وباکتری های گرم منفی به رنگ قرمز مشاهده می شود




 تئوری آزمایش
تئوری آزمایش و اتر
و اتر  با هم ایزومر گروه عاملی هستند. در ترکیبهایی دیده میشود که یک یا چند لیگاند دارای دو اتم کوئوردیناسیون دهنده باشند، برای مثال یون نیتریک NO-2 میتواند از طریق یک اتم اکسیژن یا از طریق اتم نیتروژن کوئوردیناسیون بدهد. زرد NH3)5CO(NO2)) Cl2)) و قرمز NH3)5-CO-ONO) Cl2))
با هم ایزومر گروه عاملی هستند. در ترکیبهایی دیده میشود که یک یا چند لیگاند دارای دو اتم کوئوردیناسیون دهنده باشند، برای مثال یون نیتریک NO-2 میتواند از طریق یک اتم اکسیژن یا از طریق اتم نیتروژن کوئوردیناسیون بدهد. زرد NH3)5CO(NO2)) Cl2)) و قرمز NH3)5-CO-ONO) Cl2))